Obwohl alle Atome des gleichen Elements die gleiche Anzahl an Protonen enthalten, kann ihre Anzahl an Neutronen variieren. Wenn Sie wissen, wie viele Neutronen sich in einem bestimmten Atom befinden, können Sie feststellen, ob es ein reguläres Atom dieses Elements oder ein Isotop ist, das entweder mehr oder weniger Neutronen enthalten wird.[1] Die Bestimmung der Anzahl von Neutronen in einem Atom ist ziemlich einfach und erfordert nicht einmal Experimente. Um die Anzahl der Neutronen in einem regulären Atom oder einem Isotop zu berechnen, müssen Sie nur diese Anweisungen mit einem Periodensystem in der Hand befolgen.
Methode eins von zwei:
Die Anzahl der Neutronen in einem regulären Atom finden
-
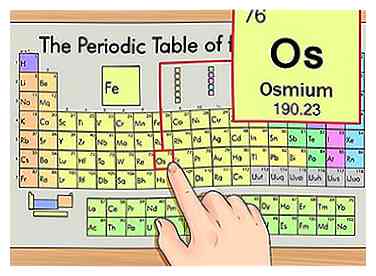 1 Suchen Sie das Element im Periodensystem. In diesem Beispiel betrachten wir Osmium (Os), das in der sechsten Reihe liegt.
1 Suchen Sie das Element im Periodensystem. In diesem Beispiel betrachten wir Osmium (Os), das in der sechsten Reihe liegt. -
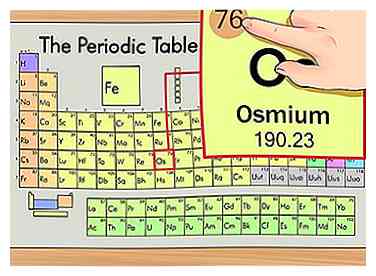 2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist normalerweise die sichtbarste Zahl für ein bestimmtes Element und befindet sich normalerweise über dem Elementsymbol, entweder in der Mitte der Box oder in der oberen linken Ecke. (Auf dem Diagramm, das wir verwenden, sind keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. Os ist Nummer 76, was bedeutet, dass ein Atom von Osmium 76 Protonen hat.
2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist normalerweise die sichtbarste Zahl für ein bestimmtes Element und befindet sich normalerweise über dem Elementsymbol, entweder in der Mitte der Box oder in der oberen linken Ecke. (Auf dem Diagramm, das wir verwenden, sind keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. Os ist Nummer 76, was bedeutet, dass ein Atom von Osmium 76 Protonen hat. - Die Protonennummer ändert sich nie in einem Element; Es ist im Grunde, was dieses Element zu diesem Element macht.
-
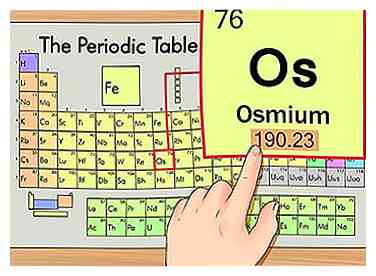 3 Finde das Atomgewicht des Elements. Diese Nummer befindet sich normalerweise unterhalb des atomaren Symbols. Beachten Sie, dass das Diagramm in diesem Beispiel nur auf der Ordnungszahl basiert und das Atomgewicht nicht aufführt. Dies wird nicht immer der Fall sein. Osmium hat ein Atomgewicht von 190,23.
3 Finde das Atomgewicht des Elements. Diese Nummer befindet sich normalerweise unterhalb des atomaren Symbols. Beachten Sie, dass das Diagramm in diesem Beispiel nur auf der Ordnungszahl basiert und das Atomgewicht nicht aufführt. Dies wird nicht immer der Fall sein. Osmium hat ein Atomgewicht von 190,23. -
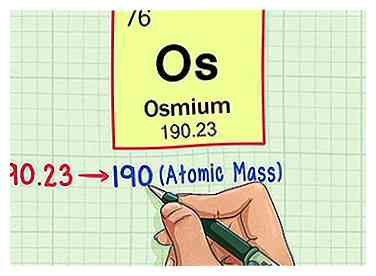 4 Runden Sie das Atomgewicht auf die nächste ganze Zahl ab, um die atomare Masse zu finden. In unserem Beispiel würde 190.23 auf 190 gerundet werden, was zu einer Atommasse von 190 für Osmium führt.
4 Runden Sie das Atomgewicht auf die nächste ganze Zahl ab, um die atomare Masse zu finden. In unserem Beispiel würde 190.23 auf 190 gerundet werden, was zu einer Atommasse von 190 für Osmium führt. - Das Atomgewicht ist ein Durchschnitt der Isotope des Elements, deshalb ist es normalerweise keine ganze Zahl.
-
 5 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms aus seinen Protonen und Neutronen besteht, ergibt das Subtrahieren der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse berechnet Anzahl der Neutronen im Atom. Die Nachkommastellen stellen die normalerweise sehr kleine Masse der Elektronen im Atom dar. In unserem Beispiel ist dies: 190 (Atomgewicht) - 76 (Anzahl der Protonen) = 114 (Anzahl der Neutronen).
5 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms aus seinen Protonen und Neutronen besteht, ergibt das Subtrahieren der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse berechnet Anzahl der Neutronen im Atom. Die Nachkommastellen stellen die normalerweise sehr kleine Masse der Elektronen im Atom dar. In unserem Beispiel ist dies: 190 (Atomgewicht) - 76 (Anzahl der Protonen) = 114 (Anzahl der Neutronen). -
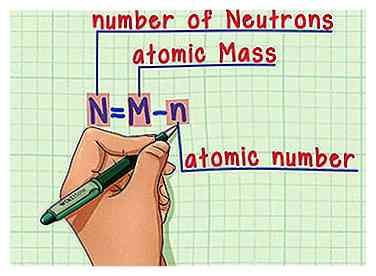 6 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel:
6 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel: - N = M - n
- N = Anzahl von Neutrons
- M = atomar MArsch
- n = atomar nUmber
- N = M - n
Methode zwei von zwei:
Die Anzahl der Neutronen in einem Isotop finden
-
 1 Suchen Sie das Element im Periodensystem. Als Beispiel betrachten wir das Kohlenstoff-14-Isotop. Da die nicht-isotopische Form von Kohlenstoff-14 einfach Kohlenstoff (C) ist, finden Sie Kohlenstoff im Periodensystem (in der zweiten Reihe nach unten).
1 Suchen Sie das Element im Periodensystem. Als Beispiel betrachten wir das Kohlenstoff-14-Isotop. Da die nicht-isotopische Form von Kohlenstoff-14 einfach Kohlenstoff (C) ist, finden Sie Kohlenstoff im Periodensystem (in der zweiten Reihe nach unten). -
 2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist tendenziell die sichtbarste Zahl, die zu einem gegebenen Element gehört, und befindet sich normalerweise über dem Elementsymbol. (In unserem Beispieldiagramm sind tatsächlich keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. C ist die Nummer 6, dh ein Atom Kohlenstoff hat 6 Protonen.
2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist tendenziell die sichtbarste Zahl, die zu einem gegebenen Element gehört, und befindet sich normalerweise über dem Elementsymbol. (In unserem Beispieldiagramm sind tatsächlich keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. C ist die Nummer 6, dh ein Atom Kohlenstoff hat 6 Protonen. -
 3 Finde die atomare Masse. Dies ist mit Isotopen, wie sie nach ihrer Atommasse benannt werden, unglaublich einfach. Zum Beispiel hat Kohlenstoff-14 eine atomare Masse von 14. Sobald Sie die Atommasse des Isotops gefunden haben, ist der Prozess der gleiche wie beim Finden der Anzahl von Neutronen in einem regulären Atom.
3 Finde die atomare Masse. Dies ist mit Isotopen, wie sie nach ihrer Atommasse benannt werden, unglaublich einfach. Zum Beispiel hat Kohlenstoff-14 eine atomare Masse von 14. Sobald Sie die Atommasse des Isotops gefunden haben, ist der Prozess der gleiche wie beim Finden der Anzahl von Neutronen in einem regulären Atom. -
 4 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms seine Protonen und Neutronen gefunden hat, wird Ihnen die Subtraktion der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse folgen berechnet Anzahl der Neutronen im Atom. In unserem Beispiel ist dies: 14 (Atommasse) - 6 (Anzahl der Protonen) = 8 (Anzahl der Neutronen).
4 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms seine Protonen und Neutronen gefunden hat, wird Ihnen die Subtraktion der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse folgen berechnet Anzahl der Neutronen im Atom. In unserem Beispiel ist dies: 14 (Atommasse) - 6 (Anzahl der Protonen) = 8 (Anzahl der Neutronen). -
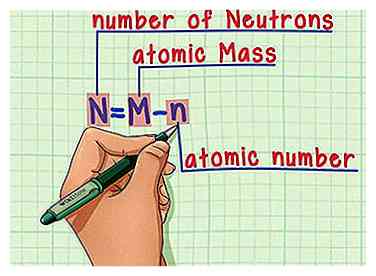 5 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel:
5 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel: - N = M - n
- N = Anzahl von Neutrons
- M = atomar MArsch
- n = atomar nUmber
- N = M - n
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Suchen Sie das Element im Periodensystem. In diesem Beispiel betrachten wir Osmium (Os), das in der sechsten Reihe liegt.
1 Suchen Sie das Element im Periodensystem. In diesem Beispiel betrachten wir Osmium (Os), das in der sechsten Reihe liegt.  2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist normalerweise die sichtbarste Zahl für ein bestimmtes Element und befindet sich normalerweise über dem Elementsymbol, entweder in der Mitte der Box oder in der oberen linken Ecke. (Auf dem Diagramm, das wir verwenden, sind keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. Os ist Nummer 76, was bedeutet, dass ein Atom von Osmium 76 Protonen hat.
2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist normalerweise die sichtbarste Zahl für ein bestimmtes Element und befindet sich normalerweise über dem Elementsymbol, entweder in der Mitte der Box oder in der oberen linken Ecke. (Auf dem Diagramm, das wir verwenden, sind keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. Os ist Nummer 76, was bedeutet, dass ein Atom von Osmium 76 Protonen hat.  3 Finde das Atomgewicht des Elements. Diese Nummer befindet sich normalerweise unterhalb des atomaren Symbols. Beachten Sie, dass das Diagramm in diesem Beispiel nur auf der Ordnungszahl basiert und das Atomgewicht nicht aufführt. Dies wird nicht immer der Fall sein. Osmium hat ein Atomgewicht von 190,23.
3 Finde das Atomgewicht des Elements. Diese Nummer befindet sich normalerweise unterhalb des atomaren Symbols. Beachten Sie, dass das Diagramm in diesem Beispiel nur auf der Ordnungszahl basiert und das Atomgewicht nicht aufführt. Dies wird nicht immer der Fall sein. Osmium hat ein Atomgewicht von 190,23.  4 Runden Sie das Atomgewicht auf die nächste ganze Zahl ab, um die atomare Masse zu finden. In unserem Beispiel würde 190.23 auf 190 gerundet werden, was zu einer Atommasse von 190 für Osmium führt.
4 Runden Sie das Atomgewicht auf die nächste ganze Zahl ab, um die atomare Masse zu finden. In unserem Beispiel würde 190.23 auf 190 gerundet werden, was zu einer Atommasse von 190 für Osmium führt.  5 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms aus seinen Protonen und Neutronen besteht, ergibt das Subtrahieren der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse berechnet Anzahl der Neutronen im Atom. Die Nachkommastellen stellen die normalerweise sehr kleine Masse der Elektronen im Atom dar. In unserem Beispiel ist dies: 190 (Atomgewicht) - 76 (Anzahl der Protonen) = 114 (Anzahl der Neutronen).
5 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms aus seinen Protonen und Neutronen besteht, ergibt das Subtrahieren der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse berechnet Anzahl der Neutronen im Atom. Die Nachkommastellen stellen die normalerweise sehr kleine Masse der Elektronen im Atom dar. In unserem Beispiel ist dies: 190 (Atomgewicht) - 76 (Anzahl der Protonen) = 114 (Anzahl der Neutronen).  6 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel:
6 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel:  1 Suchen Sie das Element im Periodensystem. Als Beispiel betrachten wir das Kohlenstoff-14-Isotop. Da die nicht-isotopische Form von Kohlenstoff-14 einfach Kohlenstoff (C) ist, finden Sie Kohlenstoff im Periodensystem (in der zweiten Reihe nach unten).
1 Suchen Sie das Element im Periodensystem. Als Beispiel betrachten wir das Kohlenstoff-14-Isotop. Da die nicht-isotopische Form von Kohlenstoff-14 einfach Kohlenstoff (C) ist, finden Sie Kohlenstoff im Periodensystem (in der zweiten Reihe nach unten).  2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist tendenziell die sichtbarste Zahl, die zu einem gegebenen Element gehört, und befindet sich normalerweise über dem Elementsymbol. (In unserem Beispieldiagramm sind tatsächlich keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. C ist die Nummer 6, dh ein Atom Kohlenstoff hat 6 Protonen.
2 Suchen Sie nach der Ordnungszahl des Elements. Dies ist tendenziell die sichtbarste Zahl, die zu einem gegebenen Element gehört, und befindet sich normalerweise über dem Elementsymbol. (In unserem Beispieldiagramm sind tatsächlich keine anderen Nummern aufgeführt.) Die Ordnungszahl ist die Anzahl der Protonen in einem einzelnen Atom dieses Elements. C ist die Nummer 6, dh ein Atom Kohlenstoff hat 6 Protonen.  3 Finde die atomare Masse. Dies ist mit Isotopen, wie sie nach ihrer Atommasse benannt werden, unglaublich einfach. Zum Beispiel hat Kohlenstoff-14 eine atomare Masse von 14. Sobald Sie die Atommasse des Isotops gefunden haben, ist der Prozess der gleiche wie beim Finden der Anzahl von Neutronen in einem regulären Atom.
3 Finde die atomare Masse. Dies ist mit Isotopen, wie sie nach ihrer Atommasse benannt werden, unglaublich einfach. Zum Beispiel hat Kohlenstoff-14 eine atomare Masse von 14. Sobald Sie die Atommasse des Isotops gefunden haben, ist der Prozess der gleiche wie beim Finden der Anzahl von Neutronen in einem regulären Atom.  4 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms seine Protonen und Neutronen gefunden hat, wird Ihnen die Subtraktion der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse folgen berechnet Anzahl der Neutronen im Atom. In unserem Beispiel ist dies: 14 (Atommasse) - 6 (Anzahl der Protonen) = 8 (Anzahl der Neutronen).
4 Subtrahiere die Ordnungszahl von der Atommasse. Da die überwiegende Mehrheit der Masse eines Atoms seine Protonen und Neutronen gefunden hat, wird Ihnen die Subtraktion der Anzahl der Protonen (d. H. Der Ordnungszahl) von der Atommasse folgen berechnet Anzahl der Neutronen im Atom. In unserem Beispiel ist dies: 14 (Atommasse) - 6 (Anzahl der Protonen) = 8 (Anzahl der Neutronen).  5 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel:
5 Erinnere dich an die Formel. Um die Anzahl der Neutronen in der Zukunft zu finden, verwenden Sie einfach diese Formel: